Bilag: Beregning af mćtningskoncentration
Mćtningskoncentrationen af oplřst ilt i vandet řnskes beregnet, da denne bruges til at beregne den reelle koncentration af oplřst ilt i vandet, ud fra de udfřrte iltmĺlinger, som vist pĺ figur I.19.1. Pĺ figuren er det illustreret hvordan den mĺlte iltkoncentration i luften svarer til mćtningskoncentrationen i vand.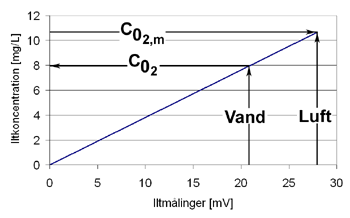
Figur I.19.1: Beregning af koncentration af ilt i vand, C02. C02,m er den mćttede koncentration af ilt i vand.
Teoretisk grundlag
Partialtryk af ilt i atmosfćren beregnes ved ligning I.19.1.Partialtryk af ilt i atmosfćren
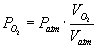
hvor
PO2 er partialtryk af ilt [atm]
Patm er atmosfćretryk [atm]
VO2/Vatm er den relative volumenandel af ilt i atmosfćren [-].
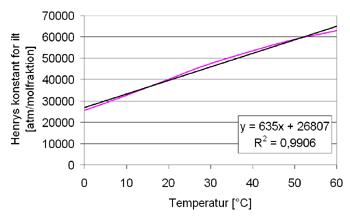
Figur I.19.2: Hensrys konstant for ilt som funktion af temperatur. [The Southwest Biotechnology and Informatics Center, 2006]
Linećr sammenhćng for Henrys konstant og temperatur
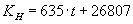
hvor
KH er Henrys konstant [atm/molfraktion]
t er temperaturen [°C].
Henrys lov
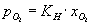
hvor
xO2 er molbrřken af ilt i vand.
Molćrkoncentrationen af oplřst ilt
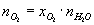
hvor
nO2 er molćrkoncentrationen af oplřst ilt [mol/L]
nH2O er molćrkoncentrationen af vand [mol/L].
Molćrkoncentrationen af oplřst ilt
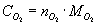
hvor
CO2 koncentrationen af oplřst ilt i vandet [mg/L]
MO2 er molvćgten af ilt [mg/mol].
Beregningseksempel
I det fřlgende er et beregningseksempel vist for d. 6. september 2006 kl. 13:00 ved station 1.872 i Hasseris Ĺ. Da bĺde temperaturen og atmosfćretrykket ćndrer sig igennem dřgnet, er der lavet en sĺdan beregning til alle mĺlingerne.D. 6. september 2006 kl. 13:00 ved station 1.872 i Hasseris Ĺ.
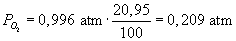
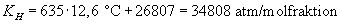
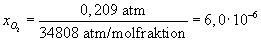
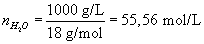
Mćtningskoncentrationen af oplřst ilt i vandet, beregnes ved ligning I.19.4 og I.19.5.
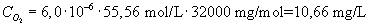
[ Til toppen ]
[ Forrige | Nćste ]